Para Bernadete Dias, sócia e head da área de Life Sciences de CGM Advogados, a reestruturação regulatória fortalece a segurança jurídica e estimula investimentos no setor.
Pela primeira vez, o Brasil passa a permitir o cultivo de cannabis em território nacional para fins medicinais e farmacêuticos. A autorização está prevista no novo marco regulatório publicado pela Agência Nacional de Vigilância Sanitária (Anvisa) na última terça-feira, 3 de fevereiro, por meio das RDCs nº 1.013/2026, 1.014/2026 e 1.015/2026. As normas reestruturam integralmente a regulação do setor, disciplinando da produção à comercialização, ampliando as formas de acesso dos pacientes e revogando a RDC nº 327/2019, que vigorava desde 2019.
“A iniciativa cumpre decisão do STJ e representa um avanço relevante para o desenvolvimento do setor medicinal e farmacêutico no país”, explica a advogada Bernadete Dias, sócia e head da área de Life Sciences de CGM Advogados, escritório de advocacia full service que atende grandes empresas do Brasil e do exterior em mais de 30 áreas do Direito Empresarial.
A autorização para o cultivo nacional é restrita e cercada de exigências. Apenas pessoas jurídicas — como empresas, universidades e associações de pacientes — poderão produzir cannabis, exclusivamente para fins medicinais e farmacêuticos. Segundo Bernadete Dias, o desenho regulatório busca equilibrar expansão do acesso e controle estatal: “O modelo prevê controle regulatório rigoroso, com rastreabilidade completa da produção e limite máximo de 0,3% de THC nas plantas”.
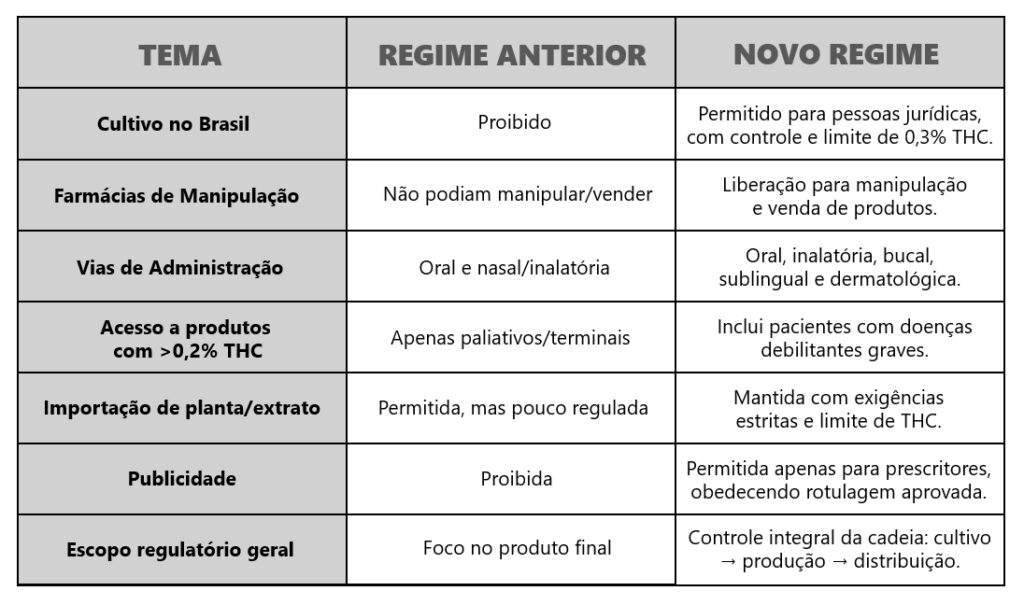
Outra mudança relevante é a inclusão das farmácias de manipulação na cadeia formal de acesso à cannabis medicinal. Com a nova regulamentação, esses estabelecimentos passam a poder manipular e vender produtos à base de canabidiol (CBD), o que tende a ampliar a capilaridade da oferta e reduzir barreiras para pacientes em diferentes regiões do país.
A Anvisa também ampliou as vias de administração permitidas. Além das formas oral e nasal ou inalatória, passam a ser autorizadas as vias bucal, sublingual e dermatológica, oferecendo maior flexibilidade clínica e potencial ganho de eficácia terapêutica.
O acesso a medicamentos com maior teor de THC também foi flexibilizado. Antes restrito a pacientes em cuidados paliativos ou com doenças terminais, agora passa a alcançar pessoas com doenças debilitantes graves, ampliando o espectro de indicações médicas possíveis.
No campo da produção e do abastecimento, a importação de plantas e extratos segue permitida, desde que respeitado o limite máximo de 0,3% de THC. A medida viabiliza um modelo híbrido de operação enquanto o cultivo nacional não atinge escala suficiente. Já a publicidade, antes totalmente vedada, passa a ser autorizada de forma restrita, direcionada exclusivamente a profissionais prescritores e limitada a informações previamente aprovadas pela Anvisa.
“O novo marco regulatório estabelece ainda um sistema robusto de controle e fiscalização, que inclui inspeção sanitária prévia, exigência de autorização especial para produção, rastreamento integral da cadeia, registro georreferenciado das áreas de cultivo e previsão de suspensão imediata das atividades e destruição do material em caso de irregularidades”, destaca a sócia de CGM Advogados.
Das três normas publicadas, a RDC nº 1.014/2026 já está em vigor e institui um Ambiente Regulatório Experimental — o chamado sandbox regulatório — para testagem controlada de atividades relacionadas à cannabis medicinal. As RDCs nº 1.013/2026, sobre cultivo, e nº 1.015/2026, que trata da fabricação, importação e comercialização, entram em vigor em 4 de maio de 2026.

























